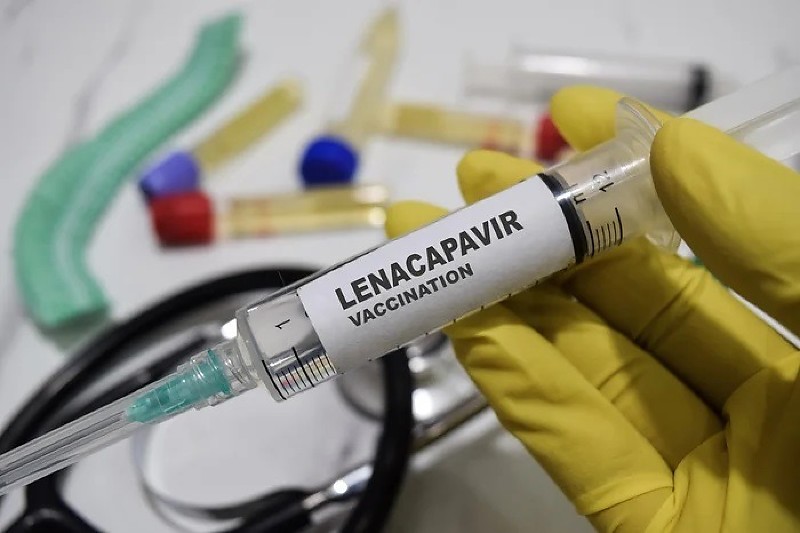
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, nesta segunda-feira (12), uma nova indicação para o medicamento Sunlenca (lenacapavir).
O fármaco agora passa a ser utilizado como Profilaxia Pré-Exposição (PrEP) para reduzir o risco de infecção pelo vírus HIV-1 por via sexual. A medida é voltada para adultos e adolescentes a partir de 12 anos, com peso mínimo de 35 kg, que estejam em grupos de risco.
O Sunlenca se destaca como um antirretroviral inovador de primeira classe. Ele atua na inibição de múltiplos estágios da função do capsídeo do vírus, o que impede a replicação e a transcrição reversa do HIV-1. O tratamento combina o uso de comprimidos orais no início do ciclo com injeções subcutâneas administradas apenas a cada seis meses, facilitando a adesão do paciente.
A aprovação no Brasil ocorre após estudos clínicos apresentarem resultados robustos de proteção. No estudo PURPOSE 1, realizado com mulheres cisgênero, o medicamento demonstrou 100% de eficácia na redução da incidência de HIV-1. Já no PURPOSE 2, a eficácia foi de 96% em comparação à incidência de base, mostrando-se 89% superior à PrEP oral de uso diário.
Em julho de 2025, a Organização Mundial da Saúde (OMS) já havia incluído o lenacapavir em suas recomendações. A entidade classifica o medicamento como a melhor alternativa preventiva disponível após uma vacina, devido ao seu regime semestral que supera os desafios de persistência comuns em esquemas de medicação diária.
O uso da PrEP é considerado uma peça-chave na chamada “prevenção combinada”. Esta estratégia integra diversas frentes de combate ao vírus, como a testagem regular, o uso de preservativos, o Tratamento Antirretroviral (TARV) e a Profilaxia Pós-Exposição (PEP). A exigência para iniciar o uso do Sunlenca é a realização prévia de um teste com resultado negativo para HIV-1.
A Anvisa ressalta que o novo regime terapêutico pode diminuir a carga sobre os sistemas de saúde, oferecendo uma ferramenta adicional para reduzir as taxas de transmissão. Com a aplicação a cada seis meses, a expectativa é que haja uma melhora significativa na continuidade do tratamento preventivo pela população-alvo.
Apesar do registro concedido pela agência reguladora, a comercialização do Sunlenca ainda aguarda etapas burocráticas. A Câmara de Regulação do Mercado de Medicamentos (CMED) deve definir o preço máximo de venda do produto no Brasil.
Quanto à oferta pública, a incorporação do medicamento ao Sistema Único de Saúde (SUS) não é automática. A disponibilização gratuita dependerá de uma avaliação técnica da Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde (Conitec) e de uma decisão final do Ministério da Saúde.
Gláucia Lima